Las auditorías de calidad son una de las principales herramientas del sistema de gestión de la calidad para comprobar el estado de cumplimiento de la normativa aplicable y proponer las medidas correctoras necesarias, independientemente de la norma de la que estemos hablando (GMP, GLP, GCP, GDP, ISO 9001, ISO 1385, ISO 22716...), o de la etapa del ciclo de vida del producto (investigación y descubrimiento, desarrollo preclínico, desarrollo clínico, fabricación de materiales de partida, fabricación de producto terminado, control de calidad, distribución, etc.).

Por lo tanto, la correcta definición del Sistema de Auditorías de Calidad es crucial para el éxito y la eficacia del proceso. En este artículo vamos a repasar los principales puntos que hay que tener en cuenta para abordar los principios del Sistema de Auditorías de Calidad y proporcionaremos algunos consejos que podrían ayudar en la gestión de las Auditorías de Calidad.
¿Qué es una auditoría?
Una auditoría es un examen metódico e independiente realizado para determinar el nivel de cumplimiento de una norma específica. Una auditoría de calidad se realiza para evaluar el diseño y la implantación adecuados de un sistema de gestión de la calidad (SGC) de acuerdo con la normativa aplicable.
Así, una auditoría proporcionará pruebas objetivas de los puntos fuertes y débiles de un SGC, y de las formas en que puede mejorarse y reforzarse.
Tipo de auditorías de calidad
Hay tres tipos principales de auditorías, según la relación entre el auditor y el auditado.
- Auditorías de primera parte, o auditorías internas. En estas auditorías, el auditor y el auditado pertenecen a la misma empresa. Estas auditorías se realizan de forma periódica, normalmente al menos una vez al año, con el objetivo de evaluar el nivel de cumplimiento del SGC y mejorar el control de los procesos internos.
- Auditorías de segunda parte, o auditorías de proveedores. Estas auditorías se realizan para evaluar el nivel de cumplimiento de los proveedores, subcontratistas o suministradores, según los requisitos externos o internos. Estas auditorías son cruciales para garantizar la calidad de los productos y servicios adquiridos externamente.
- Auditorías o inspecciones de terceros. Estas auditorías son realizadas por organismos oficiales, empresas de certificación o autoridades, para garantizar el cumplimiento de los reglamentos, normas o referencias oficiales existentes.
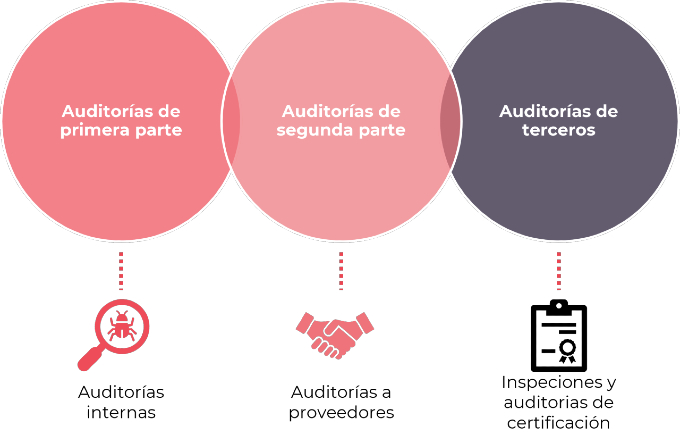
Figura 1. Tipo de auditorías
Además, en función de la norma y de la etapa del ciclo de vida del producto, las auditorías pueden realizarse con diferentes enfoques, con el fin de proporcionar la mejor evaluación del estado de cumplimiento en cada etapa. Se pueden identificar dos grupos principales de auditorías:
- Auditorías del sistema, centradas en los principios generales de la gestión, incluidos el SGC, las instalaciones y los equipos, los procesos, los sistemas informáticos, el personal, los proveedores, los documentos...
- Auditorías de productos/procesos/estudios, centradas en un área específica de preocupación, un producto específico, un proceso específico, un ensayo específico.
Veamos otra posible clasificación de las auditorías, según su método de evaluación:
- Auditorías in situ: en estas auditorías, los auditores se desplazan a las instalaciones a auditar y realizan la evaluación in situ. Esta evaluación incluye también la revisión de documentos y la entrevista cara a cara con el personal de la empresa.
- Auditorías a distancia: en estas auditorías la revisión se realiza utilizando tecnologías de comunicación, como el correo electrónico, las conferencias telefónicas o las plataformas de intercambio de información. Las instalaciones pueden visitarse electrónicamente utilizando archivos multimedia, como fotografías o vídeos. Las entrevistas con el personal se realizan mediante videollamadas o llamadas telefónicas.
- Auditoría documental: en estas auditorías la revisión se limita a los documentos y registros. No se visitan las instalaciones ni se entrevista al personal. Estas auditorías suelen apoyarse en cuestionarios o listas de comprobación que completan el auditor o los auditados y que incluyen una revisión en profundidad de los documentos y registros que aportan pruebas del cumplimiento de la normativa aplicable.
En función de la naturaleza de la auditoría, los recursos disponibles y otras situaciones condicionantes, como las restricciones de viaje, las auditorías pueden realizarse con un enfoque mixto. Por ejemplo, para reducir los días de auditoría in situ, se puede realizar una revisión documental o una auditoría a distancia como primer paso, seguida de una breve visita a las instalaciones.
Auditorías GCP
Las auditorías GCP pueden enfocarse desde tres puntos de vista:
- Auditorías a Sistemas de Gestión
- Auditorías a estudios
- Auditorías a proveedores
Veamos las particularidades de cada una de ellas.
Auditorías de sistemas (QMS)
El objetivo de este tipo de auditoría es evaluar los sistemas de garantía y control de calidad establecidos internamente para garantizar que el ensayo clínico se lleve a cabo y que los datos se generen, registren y comuniquen de conformidad con el protocolo, las BPC y los requisitos reglamentarios aplicables.
Durante la auditoría, deben revisarse los siguientes puntos:
- Organización y personal:
• Organigramas que identifican al personal clave de cada área.
• Independencia de la unidad de garantía de calidad
• Descripción de los puestos de trabajo, cualificación y formación de las personas que participan en cualquier fase del proceso del ensayo clínico
- Instalaciones y equipamiento
• Estado de calibración y cualificación de instrumentos y equipos con impacto sobre la calidad del medicamento sometido a ensayo clínico (por ejemplo, termohigrómetros o cámaras frías utilizadas en el almacenamiento)
• Control de acceso. Registro de visitantes.
• Planes de contingencia y continuidad de la actividad
• Archivo de instalaciones
- Sistema de gestión de la calidad
• Desviaciones y acciones correctivas de la auditoría anterior.
• Documentos del sistema de calidad y procedimientos operativos estándar aplicables.
• Registros de control de cambios.
• Registros de desviación.
• Registros de no conformidad e incidentes.
• Manual de calidad.
Auditoría de estudios
El propósito de una auditoría de estudio es verificar si el ensayo se ha llevado a cabo, los datos se han generado, documentado y comunicado de acuerdo con el protocolo, los principios de BPC y los procedimientos del patrocinador.
Durante la auditoría, deben revisarse los siguientes puntos:
- Protocolo y documentación
• Consentimiento informado de los sujetos del ensayo
• Notas de los pacientes
• Manual del investigador
• Manuales de estudio: muestras, CFR, SAE, gestión de PDI, análisis de laboratorio...
- Planes de estudio
• Plan de seguimiento
• Plan de gestión del proyecto
• Plan TMF
• Plan de seguridad
• Plan de gestión de datos
• Ejemplo de plan de gestión
• Plan de análisis estadístico
• Plan de gestión IMP/NIMP
- Registro del equipo de estudio
• Selección de investigadores y acuerdos
• Deberes y funciones de cada parte implicada
• Registro de personal
- Herramientas de estudio
• Tabla de registro de visitas de seguimiento
• Lista de desviaciones del protocolo
• Seguimiento de las TMF/ISF
- Informes de seguimiento
Auditoría de proveedores
Para los proveedores con impacto directo o indirecto sobre el ensayo clínico, los proveedores cuya evaluación inicial muestre la necesidad de una evaluación exhaustiva y siempre que el Departamento de Calidad lo considere oportuno, se realizará una auditoría de calidad en las instalaciones del proveedor, donde se comprobará su idoneidad para realizar las funciones contratadas. Los proveedores a considerar en este punto serán, por ejemplo, los proveedores de API para la fabricación del medicamento en investigación, los fabricantes subcontratados, CRO contratadas para la gestión del ensayo clínico, proveedores de transporte de los medicamentos en investigación a los centros o proveedores de soluciones tecnológicas (eCRF)
Esta auditoría se llevará a cabo con un enfoque diferente en función del tipo de productos o servicios proporcionados por el proveedor y de los estándares aplicables a la actividad realizada, pero teniendo siempre en cuenta los criterios GCP como elemento clave para la evaluación.
Sistema de gestión de auditorías de calidad
Las auditorías de calidad deben gestionarse considerando cuatro elementos fundamentales
- Un sistema de planificación basado en el riesgo para las auditorías que se realicen en un periodo de tiempo determinado.
- Programas eficaces de formación y cualificación de los auditores, incluyendo requisitos claros para su aprobación.
- Un sistema bien definido para planificar, realizar, informar y evaluar las auditorías.
- Un sistema eficaz para gestionar los incumplimientos hasta su cierre.
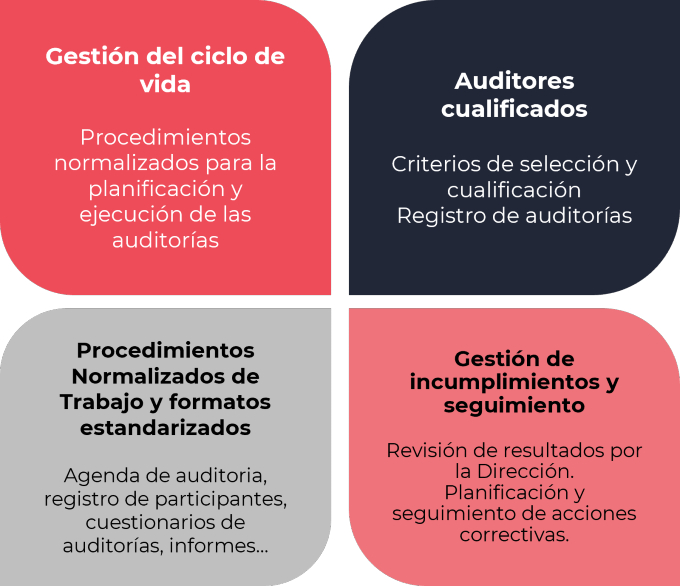
Figura 2. Elementos clave del sistema de gestión de auditorías
Ciclo de vida de las auditorías
Para mejorar la gestión de las auditorías y conseguir resultados coherentes, éstas deben gestionarse siguiendo el enfoque del ciclo de vida PDCA (véase la figura2).
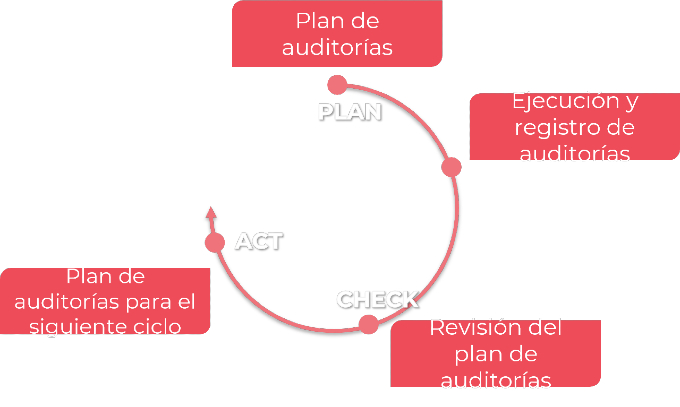
Figura 3 . Ciclo de vida de las auditorías
Plan de auditorías
Al principio de cada ciclo de auditoría, normalmente cada año, se definirá un Plan de Auditoría que incluya el tipo de auditorías que se van a realizar, su calendario, los documentos de referencia necesarios y los auditores responsables.
Se planificarán tanto las auditorías de primera parte (auditorías internas) como las de segunda parte (auditorías a proveedores y subcontratistas). Las auditorías de terceros (auditorías e inspecciones de autoridades y organismos oficiales) que se espera que se lleven a cabo en la empresa durante el Ciclo de Auditoría también podrían incluirse en el Plan, con el fin de proporcionar una visión más amplia y permitir una mejor asignación de recursos. Todas estas auditorías podrían programarse en un mismo Plan de Auditoría, o pueden prepararse diferentes Planes de Auditoría para cada tipo de auditoría.
Ejecución del plan de Auditorías
A lo largo del año, se llevarán a cabo auditorías programadas de acuerdo con los procedimientos internos y por parte de auditores cualificados. Cada auditoría realizada se registrará y se hará un seguimiento según lo descrito en las políticas de auditoría de la empresa.
Las auditorías pueden realizarse con recursos propios o pueden subcontratarse a auditores especializados o empresas de auditoría. En ambos casos, la calificación de los auditores, los procedimientos operativos y los documentos y registros generados deben estar en conformidad con las políticas internas de la empresa. Es importante recordar que este tipo de proveedores también debe incluirse en el ámbito de la evaluación y aprobación de proveedores, y puede incluirse también en el programa de auditoría.
Revisión del cumplimiento del plan
Al final de cada ciclo de auditoría, se verificará el cumplimiento del Plan de Auditoría, con el fin de comprobar que todas las auditorías programadas para ese periodo de tiempo se han realizado correctamente. En caso de incumplimiento de las disposiciones, se indicará y justificará la causa del incumplimiento.
De acuerdo con los resultados de esta revisión, se preparará el nuevo Plan de Auditoría para el siguiente ciclo de auditoría, considerando también los resultados de las auditorías realizadas. Las áreas que requieran una atención especial sobre la base de las auditorías anteriores, los informes de no conformidad o los informes de acciones correctivas se considerarán para programar auditorías adicionales.
Cualificación de los auditores
La formación y cualificación del equipo de auditores es un punto clave para conseguir los mejores resultados durante la ejecución del programa de auditoría. La calidad de la auditoría dependerá sobre todo de la experiencia y las capacidades de los auditores.
El equipo de auditores puede estar formado por cualquier empleado de la organización con la formación y cualificación adecuadas, o por auditores externos, expertos en los campos específicos de las auditorías que se van a realizar.
Los requisitos aplicables para la selección y calificación de los auditores son:
- Profundo conocimiento de las normas y reglamentos aplicables. El auditor debe ser un experto en la normativa frente a la que se realiza la auditoría. Los criterios aplicables deben estar completamente claros para el auditor, a fin de garantizar una evaluación adecuada del nivel de cumplimiento de dichos criterios.
- Conocimiento de los procesos, productos, métodos, técnicas y operaciones realizadas por la empresa auditada. La formación del auditor debe estar relacionada con las áreas de actividad de la empresa auditada, para garantizar un nivel adecuado de comprensión de los procesos a revisar.
- Formación específica en técnicas de auditoría. Sería deseable contar con certificaciones oficiales sobre estas formaciones.
- Experiencia en auditorías. A veces se puede exigir un número mínimo de auditorías realizadas durante un periodo de tiempo determinado.
- Independencia de las áreas auditadas. El auditor debe aportar un punto de vista objetivo e independiente, para garantizar la
Los auditores pueden ser personal de la empresa auditora o auditores externos, pero deberán cumplir estos requisitos en ambos casos.
Procedimientos operativos estándar y modelos de documentos
Una vez planificadas las auditorías y conformado el equipo de auditores, la realización de las mismas es también un proceso en sí mismo, y como tal ha de ser considerado y gestionado.
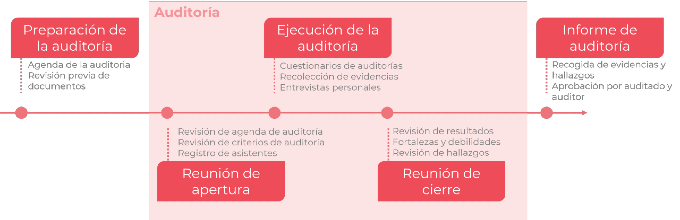
Figura 4. Proceso de auditoría
Preparación de la auditoría
Antes de realizar la auditoría, el auditor preparará una Agenda de Auditoría que se enviará al departamento/empresa auditada para informar sobre los puntos que se revisarán durante la auditoría, el calendario previsto y el personal responsable que se solicitará para cada área. La Agenda de Auditoría debe estar a disposición del auditado con suficiente antelación, para permitir su revisión y garantizar la adecuada preparación de la auditoría.
Para preparar la Agenda de Auditoría es conveniente que el auditor revise la información disponible sobre el auditado, para lograr un mejor conocimiento de la empresa y de las operaciones a auditar, como por ejemplo
- Documentos del Sistema de Gestión de Calidad aplicables al área auditada.
- Personal e instalaciones
- Actividades desarrolladas y diagramas de flujo
En caso de que se haya realizado una auditoría anterior al mismo departamento/empresa, también se debe revisar la siguiente información:
- Desviaciones y acciones correctivas abiertas en auditorías anteriores
- Modificación de los controles desde la última auditoría.
- Desviaciones e incumplimientos abiertos desde la última auditoría.
- Cambios en las actividades realizadas o en el volumen
- Cambios de personal
El auditor podría pedir la documentación necesaria antes de la realización de la auditoría, si fuera necesario.
Realización de la auditoría
La auditoría debe comenzar con una breve reunión de apertura en la que el equipo de auditores confirme el alcance de la auditoría, la norma con la que se va a realizar y la forma en que se llevará a cabo, incluidos los documentos e instalaciones que se revisarán, el personal que se entrevistará y los criterios de clasificación de los incumplimientos.
Una auditoría es, al fin y al cabo, una revisión de una muestra. Cuanto más amplia sea la muestra, más precisa será la visión. Sin embargo, una revisión del 100% del área auditada no suele ser posible. Por ello, un método de inspección planificado y sistemático es la mejor manera de optimizar el tiempo y los recursos y, por tanto, de ampliar la muestra y obtener conclusiones finales realistas.
Al realizar la auditoría, el equipo de auditores debe tener siempre presente que:
- la auditoría se realizará de forma respetuosa y profesional.
- la comunicación con el personal auditado será directa y asertiva, evitando juicios personales o comentarios subjetivos.
- la investigación debe ser exhaustiva, a fin de evaluar adecuadamente el grado de aplicación y la eficacia de los procesos.
- sólo se evaluarán las pruebas objetivas y verificadas.
- si se detecta una posible no conformidad, se investigará hasta confirmarla o no y si es accidental o sistemática.
- las no-conformidades detectadas en auditorías anteriores deben ser objeto de un estrecho seguimiento.
En ocasiones puede ser útil disponer de cuestionarios de auditoría o listas de comprobación, simplemente para asegurarse de que se revisan todas las áreas importantes, y de que el resultado de esta revisión se documenta adecuadamente. Sin embargo, esto dependerá de las preferencias del auditor y de sus prácticas de auditoría. En caso de que se utilicen, se considerarán registros de auditoría primarios, y deberán conservarse en consecuencia para garantizar su integridad durante todo su ciclo de vida.
Una vez finalizada la evaluación, el equipo auditor celebrará una reunión de cierre con el personal clave de la empresa auditada. Durante esta reunión, se compartirá con el auditado una visión general de la auditoría, incluyendo todas las áreas auditadas, los puntos fuertes y débiles detectados y los incumplimientos encontrados. Estos resultados podrán ser discutidos durante la reunión, proporcionando información adicional por parte del auditado si es necesario o explicando el motivo de la no conformidad por parte del auditor, con el fin de lograr un acuerdo entre ambas partes, que será la base para la elaboración del informe de auditoría.
El principal objetivo de esta reunión es asegurarse de que el auditado entiende claramente los principales puntos de preocupación que han surgido durante la auditoría, y que el auditor dispone de información completa y clara para preparar el informe final.
Informe de auditoría
Una vez finalizada la auditoría, el equipo auditor debe emitir el informe de auditoría. El informe debe emitirse en un plazo razonable después de la auditoría, que debe estar recogido en las políticas internas de la empresa, para asegurarse de que la información esté a disposición de los auditados lo antes posible, de modo que pueda abordarse y aprobarse el plan CAPA adecuado en el momento oportuno.
El informe incluirá la información completa sobre las áreas auditadas, la(s) fecha(s) de la auditoría, el/los auditor(es) (y, en su caso, los expertos y observadores), el objetivo y el alcance de la auditoría, los criterios de clasificación de los hallazgos y las personas de contacto implicadas en la auditoría. En el informe se debe hacer referencia a cada una de las pruebas recopiladas durante la auditoría, así como una descripción de las actividades realizadas y los comentarios de los auditores sobre el rendimiento de cada área.
Las áreas de incumplimiento se registrarán en el informe, y se clasificarán según los criterios establecidos. Se necesita una descripción específica y completa de los hallazgos para documentar plenamente el incumplimiento y permitir al auditado entender su causa y definir el plan de acción adecuado.
El Informe de Auditoría deberá ser revisado y aprobado por el auditor, y deberá ser presentado a la alta dirección, como forma de asegurar que las acciones necesarias para lograr el cumplimiento se definen e implementan adecuadamente.
Gestión de los incumplimientos y seguimiento de las auditorías
Todas las no conformidades encontradas durante las auditorías se clasificarán en relación con su impacto sobre la calidad del producto/datos, según los criterios previamente definidos. Cada no conformidad debe ser evaluada por el auditado, con el fin de encontrar la causa de la ruta y definir las acciones correctivas en consecuencia.
Se debe elaborar un plan CAPA para resolver los incumplimientos, que incluya las acciones a realizar, el personal responsable de cada una de ellas y el plazo previsto para su cierre. Se llevará a cabo un estrecho seguimiento de este plan CAPA, con el fin de asegurarse de que se mitigan los riesgos potenciales para la calidad del producto como consecuencia de los incumplimientos detectados durante la auditoría.
Es importante tener en cuenta que el objetivo de una auditoría no es sólo identificar posibles problemas, sino también resolverlos. Por ello, la definición y aplicación del plan CAPA es de vital importancia para completar el proceso de auditoría y garantizar la mejora continua.


















